Pressione di vapore: nozioni di base ed esempi
Cos'è la pressione di vapore
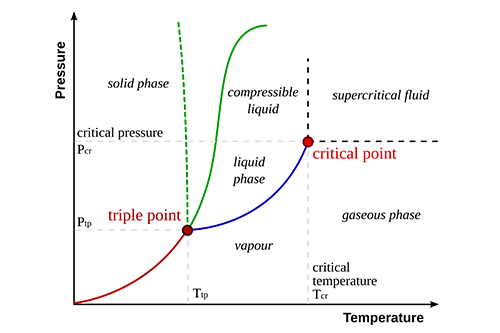
Latensione di vapore è la pressione esercitata da un vapore in equilibrio con la sua fase liquida o solida a una determinata temperatura. Indica la facilità con cui una sostanza passa da liquido a gas.
Fattori che influenzano la tensione di vapore
La temperatura
Con l'aumento della temperatura, la pressione di vapore aumenta perché un maggior numero di molecole ha l'energia per uscire dalla fase liquida.
Forze intermolecolari
Le forze intermolecolari più forti determinano una pressione di vapore più bassa, poiché le molecole richiedono più energia per vaporizzare.
Natura della sostanza
Le diverse sostanze hanno pressioni di vapore variabili in base alla loro struttura molecolare e al loro legame.
Misurazione della pressione di vapore
- Metodo manometrico: Si utilizza un contenitore sigillato con un liquido e si misura la pressione di vapore con un manometro dopo che il sistema ha raggiunto l'equilibrio.
- Metodo dinamico: le variazioni di volume o di peso del liquido vengono monitorate nel tempo per calcolare la pressione di vapore.
- Metodo dell'effusione: misura la velocità di fuoriuscita delle molecole di gas attraverso un piccolo foro, che aiuta a calcolare la pressione di vapore.
- Equazione di Clausius-Clapeyron: Utilizzata per calcolare la pressione di vapore a diverse temperature.
Importanza della misurazione della pressione di vapore
La misurazione della pressione di vapore è essenziale in diversi campi, tra cui:
- Previsioni meteorologiche: La pressione di vapore viene utilizzata per determinare l'umidità e prevedere i modelli meteorologici.
- Processi industriali: Aiuta nella distillazione, nell'evaporazione e in altri processi che comportano transizioni di fase.
- Ingegneria chimica: Svolge un ruolo nella progettazione di apparecchiature come scambiatori di calore, reattori ed evaporatori.
- Farmaceutica: le misure della pressione di vapore sono importanti per la stabilità e la conservazione dei composti volatili.
Esempi di pressione di vapore
L'acqua
A 25°C, l'acqua ha una pressione di vapore di circa 23,8 mmHg, che indica una volatilità moderata.
Acetone
L'acetone presenta una pressione di vapore superiore a quella dell'acqua alla stessa temperatura, il che lo rende più volatile.
Mercurio
Il mercurio ha una pressione di vapore molto bassa, che riflette i suoi forti legami metallici e la sua scarsa tendenza a vaporizzare.
Tabella della pressione di vapore
Ecco una tabella dei valori della pressione di vapore di varie sostanze a diverse temperature. La pressione di vapore si riferisce alla pressione esercitata dal vapore quando è in equilibrio con la sua fase liquida (o solida) a una determinata temperatura.
|
Sostanza |
Pressione di vapore a 20°C (mmHg) |
Pressione di vapore a 100°C (mmHg) |
|
Acqua |
17.5 |
760 |
|
Etanolo |
44.6 |
400 |
|
Acetone |
180 |
760 |
|
Metanolo |
95.3 |
1300 |
|
Benzene |
75.1 |
450 |
|
Etere dietilico |
430 |
5800 |
|
Mercurio |
0.0012 |
0.2 |
|
Esano |
150 |
450 |
|
Toluene |
22.3 |
230 |
|
Cloroformio |
160 |
500 |
Per ulteriori informazioni, consultareStanford Advanced Materials (SAM).
Domande frequenti
Che cos'è la pressione di vapore?
La tensione di vapore è la pressione esercitata da un vapore quando è in equilibrio con la sua forma liquida o solida.
Come influisce la temperatura sulla pressione di vapore?
L'aumento della temperatura fa generalmente aumentare la pressione di vapore, poiché un maggior numero di molecole acquista l'energia necessaria per vaporizzare.
Perché l'acqua ha una pressione di vapore inferiore a quella dell'acetone?
L'acqua ha legami idrogeno più forti e richiede più energia per vaporizzare rispetto all'acetone.
La pressione di vapore può predire la volatilità di una sostanza?
Sì, una pressione di vapore più alta indica una maggiore volatilità e una maggiore tendenza a vaporizzare.
In che modo la pressione di vapore è importante per le previsioni del tempo?
La pressione di vapore contribuisce ai livelli di umidità, influenzando i modelli meteorologici e le precipitazioni.